Forschungsschwerpunkte im AK Haberhauer
Aktuelle Forschungsschwerpunkte
In den folgenden Abschnitten stellen wir unsere aktuellen Forschungsthemen vor. In unserem Arbeitskreis beschäftigen wir uns mit der Grundlagenforschung auf verschiedenen Gebieten. Aktuelle und vergangene Ergebnisse können weiterhin der Publikationsseite entnommen werden.
Einer unserer Forschungsschwerpunkte liegt in der Gold-katalysierten Umsetzung von 1,5-Allenenen, Inamiden und halogenierten Aryl- und Alkylalkinen.
Anhand von verschiedenen Chalkogen-Motiven untersuchen wir sowohl die Ausbildung von supramolekularen Netzwerken als auch die Schaltfähigkeit von Azobenzol-Systemen.
Chalkogenbindungen – Manipulation von photophysikalischen Eigenschaften
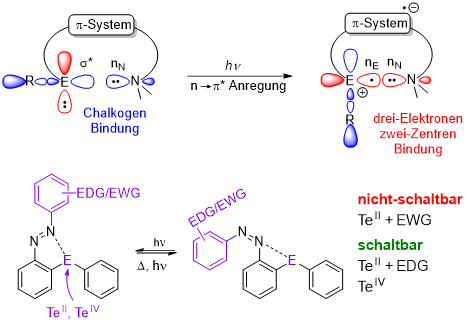
In unserem Arbeitskreis untersuchen wir, wie Chalkogenbindungen nicht nur in klassischen supramolekularen Netzwerken wirken, sondern auch im elektronisch angeregten Zustand (S1-Zustand) ihre Eigenschaften fundamental verändern. Durch Anregung mit Licht kann eine nicht-kovalente Chalkogenbindung zwischen einem Chalkogenzentrum (z. B. Tellur) und einer Lewis-Base in eine drei-Elektronen-zwei-Zentren-Bindung (3e2c-Bindung) übergehen, die deutlich stärker ist als die Bindung im Grundzustand. Diese Bindungsstärkung erklärt die unterdrückte Photoschaltbarkeit bestimmter ortho-tellursubstituierter Azoarene unter Bestrahlung. Durch gezielte Modulation der elektronischen Eigenschaften des Arylsubstituenten oder durch Änderungen des Oxidationszustands des Chalkogens lässt sich die Ausbildung dieser 3e2c-Bindung im angeregten Zustand gezielt beeinflussen. Dadurch können die photophysikalischen Eigenschaften der Azoarene signifikant verändert und ungewöhnliche Eigenschaften wie eine Temperaturabhängigkeit der photostationären Verteilung erreicht werden. Diese Arbeiten liefern Designprinzipien zur kontrollierten Nutzung von Chalkogenbindungen in lichtgetriebenen molekularen Schaltern und responsiven Materialien, indem Bindungsstärken gezielt über elektronische Anregung gesteuert werden.
Gold-Katalyse – Regio- und stereoselektive Synthese von Inenamiden
Die Knüpfung neuer C–C-Bindungen spielt in der Organischen Chemie eine wichtige Rolle. Trotzdem gibt es bisher nicht allzu viele bekannte C–C-Knüpfungsreaktionen. Eine Möglichkeit bilden übergangsmetallkatalysierte Reaktionen. Besonders interessant ist hierbei neben der Haloalkinylierung die Hydroalkinylierung von Alkinen. Diese ermöglicht die Synthese von Eninen, welche ein Grundbaustein vieler Naturstoffe sind. Wir haben uns im Arbeitskreis auf die Gold-Katalyse spezialisiert und wollten zeigen, dass auch die Hydroalkinylierungsreaktion Gold-katalysiert abläuft. Hierbei haben wir uns auf die Addition von Alkinen an Inamide konzentriert und konnten zeigen, dass diese stereo- und regioselektiv zur Bildung von Inenamiden führt. Diese Systeme sind bislang noch eher unerforscht, könnten aber aufgrund der vielseitigen Einsetzbarkeit des Enin-Gerüsts z. B. in biologisch aktiven Molekülen, interessant sein. Neben hohen Ausbeuten, konnte auch eine hohe Anwendungsbreite generiert werden.
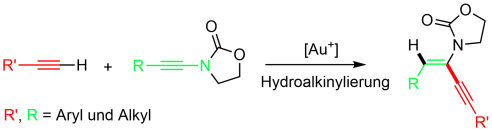
Zur Publikation: https://doi.org/10.1002/ejoc.202200591
Gold-Katalyse – Umsetzung von 1,5-Allenen-Systemen
Obwohl Gold für lange Zeit trotz seiner starken Koordinationschemie als katalytisch inaktiv galt, hat sich die Goldkatalyse in den letzten Jahrzehnten als erfolgreiches Forschungsfeld entwickelt, bei dem jährlich zahlreiche neue Entdeckungen gemacht werden. Neben Alkinen stellen hierbei Allene eins der häufigsten Strukturmotive dar, bei denen die C–C-Mehrfachbindungen durch Zusatz eines Gold-Katalysators elektrophil aktiviert werden. Wir versuchen neue C–C-Knüpfungsreaktionen von Allenen und Alkinen mit Hilfe von Gold-Katalyse zu entwickeln, die wir durch den gezielten Einsatz bestimmter funktioneller Gruppen kontrollieren wollen.
Wir konnten zum Beispiel die Gold(I)-katalysierte Reaktion von 1,5-Allenenen so kontrollieren, dass anstatt einer typischen [2+3]-Cycloaddition eine 5–exo-Cyclisierung stattgefunden hat. Dies gelang uns durch die Einführung eines Aromaten, der das Carbokation, welches im Laufe der Reaktion entsteht, stabilisiert. Letzteres konnte sowohl mit zahlreichen Sauerstoff- sowie Kohlenstoff-Nukleophilen abgefangen werden. Mit dieser Methode konnten wir tricyclische Grundgerüste mit exzellenter Chemo- und Diastereoselektivität herstellen. Den Mechanismus der Reaktion haben wir zusätzlich über quantenchemische Rechnungen untersucht.
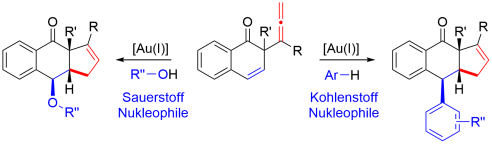
Zur Publikation: https://doi.org/10.1021/acs.orglett.1c03886
